-
Randevu ve İletişim
- 0546 554 10 20
Randevu, Teşhis ve Tedavi için İletişime Geçiniz.
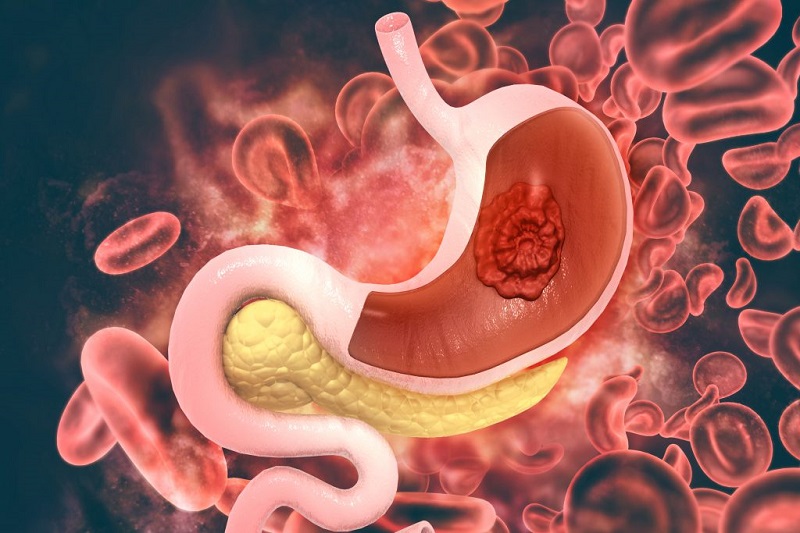
Mide sindirim sisteminde yutak borusu ile oniki parmak bağırsağı (duodenum) arasında yer alan bir organdır. Yemekler burada toplanarak mide asidi ile ön sindirimden geçerler. Mide duvarı son derece kalındır ve beş katmandan meydana gelir. Mide kanserleri mide içini saran mukoza adı verilen zardan köken alır. Kanser büyüdükçe bu astarı geçerek önce altındaki destek dokusuna, sonra kalın kas tabakasına geçer. En son seroza adı verilen en dış tabakayı geçerek komşu organlara yayılır. Mide büyük bir organ olduğu ve duvarı kalın olduğu için bulgu vermeden büyük boyutlara ulaşabilir. Karın içi zarı (periton) yayılımı sık görülür. Bu nedenle hastaların önemli bir kısmında teşhis edildiklerinde, bu yollarla lokal veya uzak yayılım söz konusudur. Mide kanserlerinin çoğu ülser şeklindedir ve iyi huylu mide ülseri görünümünde olabilirler. Ancak ülserin 2 cm`den büyük olması ve kenarlarının yüzeyden kabarık olması gibi özellikler kanser ihtimalini düşündürür.
Mide kanserleri batı ülkelerinde azalmasına rağmen doğu ve uzak doğuda halen en sık görülen kanserler arasında yer almaktadır. Mide kanseri görülme sıklığının yüksek olduğu ülkelerden, düşük olduğu ülkelere göç eden insanlarda bu kanserin görülme sıklığında dikkate değer azalma tespit edilmiştir. Örnek olarak yapılan çalışmalarda Japonya’dan Amerika'ya göç edenler arasında, yeni ülkede doğup büyüyenlerde azalma açıkça ortaya çıkmaktadır. Bunda göç eden nüfusun zamanla diyet alışkanlığını değiştirmesinin ve yeni toplumlarının yemek kültürlerine uymalarının çok önemli bir rolü vardır. Ayrıca göç edilen ülkenin çevresel faktörleri de dikkate alınmalıdır.
Mide kanserleri erkeklerde kadınlara göre 2 misli daha sık ortaya çıkar. Kırk yaşından itibaren de artan yaşla beraber insidansında bir artış görülür ve 60-70 yaş arasında en yüksek seviyelerine çıkar. Mide kanseri genellikle ileri evrelerde teşhis edildiği için kanser ölümleri arasında önemli yer tutar.
Mide kanserine sebep olduğu düşünülen en önemli risk faktörleri diyet ile ilgili olanlardır. Diyet alışkanlığı ile mide kanseri arasında yakın bir ilişki vardır. Gıdaları uzun süre muhafaza etmek için kullanılan nitrat ve nitritlerin mide kanseri riskini artırdığı düşünülmektedir. Taze sebze ve meyveden fakir, vitamin A ve vitamin C içermeyen diyetle beslenme riski artırır.
Ayrıca kızartmalar, tütsülenmiş, kurutulmuş, tuzlanmış yiyeceklerle, özellikle bu işlemlerden geçirilmiş balık yemekle riskin arttığı gösterilmiştir. Tütsülenmiş balık ürünlerinin mutasyona sebep olduğu ve vitamin C ile bu mutasyonların oluşumunun önlenebildiği de gösterilmiştir. Taze meyva ve sebzelerin koruyucu etkileri ortaya konmuştur. Aynı şekilde buzdolabı kullanımının ve dondurarak saklama yöntemlerinin gelişmesinin mide kanseri sıklığında azalmaya sebep olduğu belirtilmektedir.
Mide kanseri oluşumunda çevresel, genetik ve ailesel faktörler sebep olarak gösterilmektedir. Tütün ve tütün ürünleri kullanımı, aile öyküsü, erkek cinsiyet, beyaz ırk, A kan grubu, yaşlılık, düşük sosyoekonomik statü ve geçirilmiş mide ameliyatları mide kanseri riskini artırır. Ülser veya delinme gibi kanser dışı problemler nedeniyle midenin bir kısmının alındığı hastalarda 15-20 yıl içinde kalan mide dokusunda kanser oluşabilmektedir. Ameliyat sonrasında midenin üst ve alt kapaklarının alınması veya görev yapamaz hale gelmesi nedeniyle safranın mideye geri kaçması veya mide asitinde azalmanın buna sebep olabileceği düşünülmektedir. Mide asit üretiminin azaldığı aklorhidri, atrofik gastrit gibi klinik durumlar veya mide duvarında oluşan polipler ve intestinal metaplazi gibi değişiklikler mide kanserine yol açabilir. Diğer çevresel ve kişisel nedenler arasında kurşun, nikel, kömür, lastik ve asbest maruziyeti sayılabilir.
Helikobakter pilori infeksiyonu önemli bir sebepsel faktördür. Helikobakter pilori infeksiyonunun gastritli ve ülserli hastalarda sık görülmesi nedeniyle mide mukozal hasarı ve bunun sonucunda gelişen atrofik gastrite bir zemin hazırlayabileceği düşünülmektedir. Bakteriyal enfeksiyon nedeniyle lokal olarak salınan nitrozaminler gibi bileşiklerin mide kanseri oluşumuna katkıda bulunabileceği düşünülmektedir.
Mide kanserlerinde hastaların en sık görülen şikayetleri karın üst bölgesinde belli belirsiz rahatsızlık hissi, yanma, ekşime, ağrı, iştahsızlık ve kilo kaybıdır. Yutma güçlüğü, bulantı, kusma, kansızlık ve kansızlığa bağlı halsizlik, yorgunluk gibi belirtilere de sıklıkla rastlanır. Daha ileri aşamada şişkinlik, yutma güçlüğü, karın ağrısı veya erken doyma hissi ortaya çıkar. Hastaların bir kısmı mide kanaması, karın içinde su toplanması, sarılık veya ele gelen kitle ile gelir. Belirtiler kanserin mide içinde yerleşim yerine göre değişebilir. Örneğin yutak borusu ile bileşim yerinde yerleşmiş bir tümörde yutma güçlüğü ön planda iken, midenin çıkışında yerleşmiş tümörde tıkanma ve midede genişlemeye bağlı bulgular belirgindir.
Mide sindirim sistemini oluşturan organlar içerisinde duvarı en kalın ve iç boşluğu en geniş organdır. Bu özellikleri nedeniyle mide tümörleri teşhis edilmeden önce uzun süre belirti vermeden büyüyüp yayılabilirler. Mide kanserlerinin erken evrelerde belirti vermemesi veya çok belirsiz semptomlarla seyretmesi erken tanıyı zorlaştırır. Bu nedenle hastaların geçici olmayan tüm şikayetleri, hafif de olsa, araştırılmaya değer bulunmalıdır. Mide kanserlerinde erken teşhis edilen hastalarda cerrahi ile kür şansı çok yüksektir.
Endoskopi mide kanseri teşhisi için altın standarttır. Halk arasında "mideye hortum atma" olarak bilinen bu yöntemde yaklaşık 1 cm çapındaki bir esnek boru ile mide iç yüzeyi görüntülenir. Bir bulgu tespit edilmesi durumunda ucunda klips olan bir tel yardımı ile biyopsi yapılabilir. Abdominal ultrasonografi hem primer hastalığın teşhisinde hem de karaciğer metastazı gibi yayılımların tespitinde faydalı olabilir. Endoskopik ultrasonografi de artık giderek daha sık kullanılmaya başlamıştır. Özellikle erken mide kanseri teşhisinde primer tümörün midenin hangi katlarına yayılmış olduğunu gösterme yönüyle (T evresi), etkin bir noninvazif yöntemdir. Lenf nodu tutulumunu gösteren en iyi yöntemdir. Bunun dışında tümörün yayılıp yayılmadığını tespit amacıyla bilgisayarlı tomografi ve PET-BT kullanılmaktadır.
Mide kanseri tedavisinde cerrahi, radyoterapi ve kemoterapi tek başlarına veya birlikte kullanılmaktadır. Erken mide kanserlerinde (tümör mukoza ve submukozada sınırlı) tek başına cerrahi ile tam iyileşme şansı vardır. Bu amaçla yapılan geniş cerrahi sonrası mide kanserinde koruyucu (adjuvan) kemoterapi ve radyoterapi ile hayatta kalma ihtimali artmaktadır. Metastatik ileri evrede kemoterapi palyatif amaçlı uygulanmaktadır. Genel olarak mide kanserleri artık kemoterapiye duyarlı kanserler arasında yer almaktadır.
Mide kanserlerinde cerrahi temel tedavi olarak kabul edilir. Billroth'un 1881'de mide kanserine başarılı bir kısmi ameliyat (gastrektomi) uygulamasıyla bu hastaların tedavisinin mümkün olabileceği görüşü ortaya atılmıştır. Günümüzde total gastrektomi yapmak yerine; tümörün lokalizasyonu ve büyüklüğüne göre midenin etkilenen kanserli kısmının alınmasının (parsiyel veya subtotal gastrektomi) yeterli olduğu kabul edilmektedir. Cerrahinin işinde ehil ve tercihan sadece mide-barsak sistemi kanserleriyle uğraşan cerrahlar tarafından yapılması en uygunudur. Mide etrafındaki lenf bezlerinin de çıkarılması optimum bir cerrahi için gereklidir. Yöntem olarak mide yakın çevresi (D1) lenf bezlerine ilave olarak dalak çevresi ve dalağa ve karaciğere giden damarlar çevresindeki (D2) lenf bezlerinin de temizlenmesi gereklidir. Daha ilerideki lenf bezlerinin (D3 ve D4) çıkarılması gerekli değildir ve komplikasyonlara sebep olarak hastanede kalış ve yoğun bakım sürecini uzatır.
Erken evre mide kanserinde koruyucu (Adjuvant) kemoterapi:
Koruyucu kemoterapinin gerekçesi cerrahi sonrası rezidü lokal veya mikroskopik metastatik hastalığı ortadan kaldırmak ve nüks ihtimalini azaltmaktır. Çok erken tümörler hariç, cerrahi olarak tam çıkartıldığı düşünülen, özellikle lokal ilerlemiş fakat ameliyat edilebilir tümörlerde (T3-T4, N1-N2, M0) koruyucu kemoterapi mutlaka verilmelidir. Koruyucu kemoterapi ile nüks riski yaklaşık %40-45 oranında azalmaktadır.
Lokal ileri evre mide kanserinde cerrahi öncesi (Neoadjuvant) kemoterapi:
Ameliyat öncesi tomografi, PET veya endoskopik ultrasonografi ile mide çevresinde büyümüş metastatik lenf bezlerinin görüldüğü hastalarda, ameliyat öncesi kemoterapi ile tümörün küçültülerek cerrahiye daha uygun hale getirmek son zamanlarda daha ön plana çıkmıştır. Özellikle lokal ileri sınırda tümörlerde ve lenf nodu metastazı şüphesinde ameliyat öncesi kemoterapi artık uluslararası tedavi kılavuzlarında önerilmekte ve ülkemizde de giderek daha sıklıkla uygulanmaktadır. Ancak bu hastalarda %10-15 oranında tümörün kemoterapi alırken büyüme riski olduğu da unutulmamalıdır. Bu amaçla port takılarak FLOT (5FU + folinik asit + docetaksel + oksaliplatin) şeması en sık kullanılan kemoterapi protokolüdür.
İlerlemiş mide kanserlerinde kemoterapi:
Kombine kemoterapide en çok platin ve 5-FU içeren kombinasyonlar kullanılmıştır. En sık kullanılan kombinasyon cisplatin ve 5-FU/kapesitabin şemasıdır. Cisplatin yerine oksaliplatin yerleştirilmesiyle elde edilen CAPOX/XELOX şeması daha düşük yan etki profili ile hastalar tarafından iyi tolere edilmekte ve son yıllarda giderek popüler hale gelmektedir. Sonuç olarak ilerlemiş mide kanserlerinde mevcut kemoterapi şemalarıyla %70-80`lere varan hastalık kontrol oranları bildirilmiştir.
Mide kanserlerinde cerrahi sonrasında koruyucu (adjuvant) olarak radyoterapi verilebilir. Burada amaç, lokal-bölgesel nüks riskini azaltmaktır. Özellikle lenf nodu tutulumu varsa nüks açısından risk yüksektir. Bu nedenle bu hastalara cerrahi sonrası koruyucu kemoterapiye ilave olarak radyoterapi verilmesi önerilmektedir. D2 diseksiyonu ile mide çevresindeki gerekli lenf bezlerinin tamamen çıkarıldığı hastalarda radyoterapi yapılmayabilir. Radyoterapi, cerrahi şansı olmayan hastalarda primer tedavi olarak da kullanılmaktadır, 4500-6000 cGy dozlarında semptomatik iyileşme ve uzun sağkalım söz konusu olabilir.
Kanserin moleküler temelini daha iyi anlamak hücre farklılaşmasını, çoğalmasını ve yaşamını etkileyen hedefe yönelik tedavilerin gelişmesini sağlamıştır. Epidermal büyüme faktörü reseptör (EGFR) ailesinden olan HER2 (c-Erb-B2) onkogenine karşı trastuzumab isimli protein antikoru geliştirilmiştir. Trastuzumab'ın kemoterapiye eklenmesiyle, HER2 pozitif metastatik mide kanserinde sağkalımı uzattığının kanıtlanması son yıllarda bu alandaki en önemli gelişmedir.
HER2 pozitif metastatik mide kanserinde yapılan randomize faz 3 TOGA çalışmasında hastaların %22,1’inde HER2 pozitifliği saptanmıştır. Özellikle immünhistokimya 3+ veya 2+/FİSH+ hastalarda tedaviye trastuzumab eklenmesiyle belirgin sağkalım üstünlüğü tespit edilmiştir. Trastuzumab alan hastalarda tedaviye yanıt oranı kemoterapi koluna göre daha yüksektir. Kemoterapiye trastuzumab eklenmesi ilave bir toksisite artışına neden olmamıştır. Bu çalışmanın bulguları metastatik mide kanserlerinde trastuzumab tedavisinin uygulanabilecek olduğu grubun tespitini sağlaması yanında HER2 pozitifliğinin klinik değerlendirilmesini de kolaylaştırmıştır.
Ülkemizde Her2 pozitifliği oranı %13-18 arasındadır. Ancak T.C. Sağlık Bakanlığı trastuzumab kullanımı için Her2 pozitifliğinin tespitinde immünhistokimya metodunun yanısıra FISH testi ile konfirme edilmesini zorunlu tutmuştur.
"Ramucirumab" isimli bir monoklonal antikor tümörün kan damarlanmasını bozarak ve yeni damarlanma oluşumunu düzenleyerek (angiogenesis) etki eder. İlerlemiş mide kanseri 2. basamak ve sonrasında kemoterapiye eklenmesinin hastaların yaşam süresini uzattığının gösterilmesinden sonra Batılı ülkelerde rutin tedavinin bir parçası haline gelmiştir. Ülkemizde ruhsatlı değildir, ancak özel izin ile kullanımı mümkün olabilmektedir. İmmünoerapi tedavisi metastatik mide kanserli bazı hastalarda (PD-L1 pozitif veya mikrosatellit instabil) kemoterapi sonrası nüks durumunda uluslararası kılavuzlarda önerilmektedir. Ancak bu hastalarda kullanımının ülkemizde ruhsatı yoktur ve geri ödemesi yapılmamaktadır.
Kanser tedavisi sırasında ve sonrasında iyi beslenmek önemlidir. Yeterli miktarda kalori ve protein ihtiyacının karşılanması hastanın kendini daha iyi hissetmesine yardımcı olabilir. Mide kanseri cerrahisinden sonra kilo kaybı sıktır. Midenin bir kısmı veya tamamı alındığından sindirim problemleri baş gösterebilir. Tüketilen yiyeceklerin türü ve şeklinin değiştirilmesi gerekebilir. Mide ameliyatı sonrası veya kemoterapi/radyoterapi sırasında beslenmek zor olabilir. İştahsızlık, bulantı veya kusma tedavilere eşlik edebilir. Tat duyusunda bozulma veya azalma, iştahsızlık ve yeme isteğinde kayıba sebep olabilir.
Mide ameliyatından sonra sık görülen bir problem Dumping sendromudur. Dumping sendromu "hızlı mide boşalması" olarak da bilinir ve mideye giren yiyeceklerin hızlı bir şekilde bağırsaklara geçmesi sonucu meydana gelir. Genellikle çok hızlı ve fazla yiyecek alımı sonrası görülür. Bu problem yiyecek veya sıvılar ince bağırsağa çok hızlı geçtiklerinde olur. Hastalarda kramplara, bulantı, şişkinlik, ishal ve baş dönmelerine sebep olabilir. Az az ve sık yemek bu durumun önlenmesine yardımcı olabilir. Ayrıca midenin bir kısmı alındığından emilimi azalan vitamin B12'nin kalçadan iğne yoluyla verilmesi sık yapılan bir tedavidir. Dodex isimli vitamin B12 desteğinin yükleme sonrası ayda bir kere ömür boyu sürdürülmesi gerekir.
Mide kanserinde tarama hastalığın çok sık görüldüğü Kore ve Japonya'da özel yöntemler, boyalar ve floresan ışıklı endoskopi kullanılarak yapılmaktadır. Serum pepsinojen seviyelerinin ölçülmesi de öneriler arasındadır. Ancak bu yöntemlerin Uzakdoğu dışındaki ülkelerde mide kanserinin erken teşhisine ve yaşam süreleri üzerine bir katkısı gösterilememiştir. Günümüzde mide kanseri için rutin tarama önerilmemektedir.
Baykara M, Benekli M, Ekinci O, Irkkan SC, Karaca H, Demirci U, Akinci MB, Unal OU, Dane F, Turkoz FP, Balakan O, Eser EP, Ozturk SC, Ozkan M, Oksuzoglu B, Sevinc A, Demir N, Harputluoglu H, Yalcin B, Coskun U, Uner A, Ozet A, Buyukberber S; Anatolian Society of Medical Oncology (ASMO). Clinical significance of HER2 overexpression in gastric and gastroesophageal junction cancers. Journal of Gastrointestestinal Surgery 2015;19(9):1565-1571.
Ciltas A, Buyukberber S, Topcu TO, Kucukoner M, Uyeturk U, Cihan S, Sendur MA, Budakoglu B, Kefeli U, Yildiz R,Goksel G, Berk V, Balakan O, Oksuzoglu B, Uncu D, Ozdemir F, Benekli M. Efficacy and Toxicity of Cisplatin and Capecitabine Combination in the First-Line Treatment of Patients with Advanced Gastric Cancer: A Multicenter Study by the Anatolian Society of Medical Oncology. UHOD 2015;26:96-102.
Gumusay O, Benekli M, Ekinci O, Baykara M, Ozet A, Coskun U, Demirci U, Uner A, Dursun A, Atak EY, Buyukberber S. Discordances in Her2 status between primary gastric cancer and corresponding metastatic sites. Japanese Journal of Clinical Oncology 2015;45:416-421.
Sendur MA, Ozdemir N, Özatlı T, Yazıcı O, Aksoy S, Ekinci AS, Yazılıtaş D,Günaydın Y, Oksuzoglu B, Benekli M, Zengin N. Comparison the efficacy of second-line modified EOX (epirubicin, oxaliplatin, and capecitabine) and irinotecan, 5-fluorouracil, and leucovorin (FOLFIRI) regimens in metastatic gastric cancer patients that progressed on first-line modified docetaxel andcisplatin plus fluorouracil (DCF) regimen. Medical Oncology 2014;31(9):153.
Tonyali O, Benekli M, Karakan T, Kerem M, Dursun A, Coskun U, Buyukberber S. Primary squamous cell carcinoma of the stomach. UHOD 2014;24:219-220.
Alici S, Buyukberber S, Alkis N, Benekli M, Ozkan M, Bilici A, Demirci U,Karaca H, Arpaci E, Gumus M, Altunbas M, Dane F, Turk HM; Anatolian Society ofMedical Oncology. Low-dose docetaxel/cisplatin - leucovorin and 46 hour infusional fluorouracil in metastatic gastric carcinoma. Asian Pacific Journal of Cancer Prevention 2013;14(1):423-7.
Kucukoner M, Isikdogan A, Arpaci E, Bilici M, Uncu D, Cetin B, Dane F, Inanc M, Kaplan MA, Cayir K, Yetisyigit T, Ozdemir N, Inal A, Aksoy S, Alkis N, Tekin SB, Eroglu C, Turhal S, Benekli M, Buyukberber S. Adjuvant chemoradiation for gastric cancer: Multicentric study of the Anatolian Society of Medical Oncology. Hepatogastroenterology 2012;59:2343-2347.
Kaya AO, Coskun U, Gumus M, Dane F, Ozkan M, Isıkdogan A, Alkis N,Buyukberber S, Yumuk F, Budakoglu B, Demirci U, Berk V, Bilici A, Inal A, Arpacı E, Benekli M; Anatolian Society of Medical Oncology (ASMO). The efficacy and toxicity of irinotecan with leucovorin and bolus and continuous infusional 5-fluorouracil (FOLFIRI) as salvage therapy for patients with advanced gastric cancer previously treated with platinum and taxane-based chemotherapy regimens. Journal of Chemotherapy 2012;24(4):217-220.
Yildiz R, Kalender ME, Dane F, Sevinc A, Gumus M, Camci C, Alici S, Kaya AO, Yaman E, Öztürk B, Coskun U, Benekli M, Uncu D, Buyukberber S. Docetaxel combined with oral etoposide as second-line treatment for advanced gastric carcinoma after failure of platinum- and fluoropyrimidine-based regimens. Journal of Oncology Pharmacy Practice 2010;16:173-178.
Yaman E, Coskun U, Sancak B, Buyukberber S, Ozturk B, Benekli M. Serum M30 levels are associated with survival in advanced gastric carcinoma patients. International Immunopharmacology 2010;10(7):719-22.
Benekli M, Güllü İH, Tekuzman G, Savaş MC, Hayran M, Hasçelik G, Fırat D. Circulating intercellular adhesion molecule-1 and E-selectin in gastric cancer. British Journal of Cancer 1998;78:267-271.
Öztürk MA, Benekli M, Güler N, Altundağ MK, Barışta İ, Ayhan A. Gastric adenocarcinoma metastasis to the parotid gland. Journal of Clinical Gastroenterology 1997;25:698-699.
Şahin S, Hindioğlu U, Benekli M, Sivri B, Sökmensüer C, Sungur A. Peculiar inflammatory cutaneous metastasis from stomach adenocarcinoma. British Journal of Dermatology 1997;136:650-652.
Copyright @2020 Her Hakkı Saklıdır. Site içerisindeki görseller ve dökümanlar kopyalanamaz, çoğaltılamaz. Reklamfoni